CO2が酸でHCO3-がアルカリである理由
【体液pHが一定に保たれる理由】
細胞が適切に働くには体液を至適pHに保つ必要があるが、体内は代謝によって産生される多量のCO2などの揮発性酸と乳酸、リン酸、ケトン体などの不揮発性酸のために酸性になる傾向にある。
体が酸性に傾きすぎないように酸を排出してpHを維持する緩衝系がある。酸であるCO2と塩基であるHCO3-を肺と腎臓でコントロールしている(重炭酸緩衝系という)。肺は呼吸を介して、腎臓は尿を介して体の外とつながっているため、効率よくpHを調整することができる。
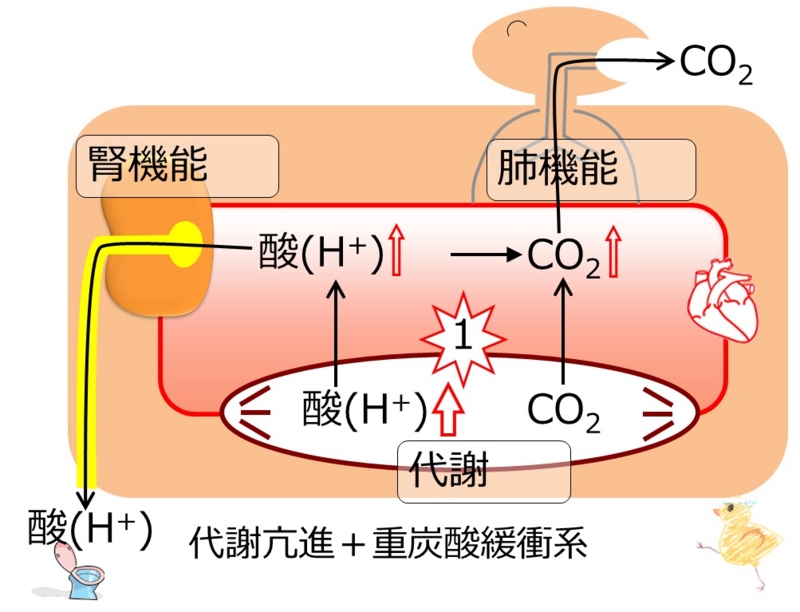
(一歩一歩学ぶ生命科学より)
【CO2が酸、HCO3-が塩基なのは何故?】
CO2+H2O→H++HCO3-
(CO2が増えると水と反応してH+を生み出す。故にCO2は酸と考える)
CO2+H2O←H++HCO3-
(HCO3が増えるとH+を消費して水とCO2にしてしまう。よって酸(H+)を減らすからHCO3-はアルカリと考える)
■ヘンダーソンの式とは
血液のpHは次のヘンダーソンの式を用いて計算することができる。
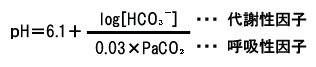
代謝性因子:腎臓で調節される、呼吸性因子:肺で調節される
(HCO3-の単位はmEq/L、PaCO2の単位はmmHgである)
この式より、血中HCO3-と動脈血中の二酸化炭素分圧PaCO2の値によって血中のpHが近似的に求められることがわかる。
尚、基準値は以下の通り。
pH=7.35-7.45
PaCO2=35-45mmHg
HCO3-=22〜26mEq/L